|
Derivado de CaseIt - un proyecto apoyado por NSF en la Universidad de Wisconsin-River Falls ( http://www.caseitproject.org/ ) Antecedentes de la enfermedad: distrofia muscular de Duchenne (DMD) en una forma de distrofia hereditaria ligada al cromosoma X que afecta principalmente a los hombres. Los síntomas de DMD incluyen debilidad muscular esquelética progresiva y severa con pérdida de células musculares y reemplazo con tejido adiposo. Una mutación común asociada con DMD es la eliminación de una o más regiones en el ADN que codifican la proteína distrofina. Estas deleciones pueden detectarse mediante digestión con enzimas de restricción y un método llamado transferencia Southern utilizando una combinación de sondas que son complementarias de múltiples regiones codificadoras de distrofina. Antecedentes de la transferencia Southern: la digestión con enzimas de restricción genera un conjunto de fragmentos reproducibles a partir del ADN, pero identificar el fragmento de interés puede ser un desafío. Edwin Southern desarrolló un método que permite la identificación de secuencias específicas complementarias a una sonda seleccionada. El ADN se extrae de las células, se digiere con enzimas de restricción, y los fragmentos se separan por electroforesis en poliacrilamida o agarosa (Nota: Hasta ahora, esto es como el análisis RFLP).
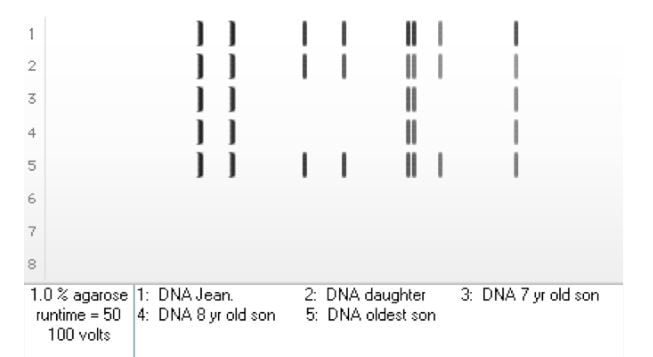
Sin embargo, en lugar de observar todas las bandas que se generarían a partir de una muestra de ADN completa, si se conoce la secuencia de fragmentos de interés (al menos parcialmente), es posible la hibridación para identificar las secuencias de ADN. Por lo tanto, Southern desnaturalizó los fragmentos de ADN en el gel y transfirió el ADN ss resultante a una membrana. La membrana luego se seca para asegurar la unión y luego se expone al ADN complementario a las regiones de interés ("sonda de ADN") que es detectable por fluorescencia o radioactividad en condiciones que permiten que las regiones complementarias se hibridicen. Se elimina el exceso de ADN de la sonda, y cuando la sonda se ha hibridado será detectable para identificar fragmentos que son complementarios a la sonda. Caso: Jean y Bill tienen tres hijos, de 12, 8 y 7 años, y una hija de 6 años. El hijo mayor y la hija están sanos, pero los dos hijos más pequeños muestran síntomas de debilidad muscular que concuerdan con la distrofia muscular temprana. Jean sabe que tiene antecedentes familiares de distrofia muscular, pero no sabe si es portadora del gen de la enfermedad. Ella busca pruebas de ADN para determinar si sus hijos menores pueden haber heredado la forma del gen de la distrofina asociada con la distrofia muscular de Duchenne (DMD). También quiere saber si su hija es portadora de este gen. El gen que codifica la distrofina se encuentra en el cromosoma X; así, los machos tienen una sola copia, mientras que las hembras tienen dos copias. Una mujer que tiene una sola copia del gen de la distrofina DMD es un "portador" de la enfermedad y puede transmitirla a sus hijos varones y mujeres. Sin embargo, los niños varones que heredan el gen de la distrofina DMD desarrollarán la enfermedad, mientras que las niñas serán portadoras si heredan el gen de la distrofina DMD (a menos que su padre esté afectado por la enfermedad y la madre pase el gen de la distrofina DMD como portador). - una ocurrencia rara debido a la aparición temprana de síntomas de la enfermedad en niños varones). Para llevar a cabo una transferencia Southern para evaluar a los miembros de la familia, cada muestra de ADN se digiere con Hind III, los productos de digestión se separan en un gel de agarosa, los productos separados se transfieren a una membrana y la membrana se sondea con las sondas de ADN apropiadas etiquetadas para visualice donde este ADNss hibridó con la muestra de ADN. Muestras de ADN examinadas: 1. Jean (madre) 2. hija 3. hijo de 7 años 4. hijo de 8 años 5. hijo mayor Preguntas: Según el número y el tamaño de los fragmentos unidos por la especie de sonda, determine el estado de cada uno de los individuos evaluados: ¿Cuál es el estado de Jean? Negativo para la enfermedad homocigota Para su hija? Negativo para la enfermedad homocigota ¿Para su hijo de 7 años? Positivo para enfermedad ¿Para su hijo de 8 años? Positivo para enfermedad ¿Para su hijo mayor? Negativo para enfermedad El hijo mayor no es portador de la enfermedad, mientras que los hijos de 7 y 8 años tienen patrones diferentes que indican la presencia de la enfermedad. La hija no tiene enfermedad homocigótica. Los resultados de la transferencia Southern son diferentes para los hijos de 7 y 8 años, por lo que podemos concluir que tienen la enfermedad. ¿Qué conclusiones puedes sacar de estos resultados? La mutación DMD da como resultado la eliminación de una región de codificación (que conduce a los fragmentos que faltan en el análisis Southern). DMD está vinculado a X, por lo que Jean debe ser portadora, y su hija también puede ser portadora, ya que la intensidad de sus bandas en las regiones que faltan en los dos hijos menores es similar a la del hijo mayor (que solo tiene uno gen de tipo salvaje en su único cromosoma X). Si Jean y su hija no fueran portadoras, las bandas que faltan en los hijos afectados por DMD serían más intensas porque las mujeres tienen dos cromosomas X. Sin embargo, una prueba cuidadosa para confirmar el estado del transportista para la hija sería importante. Esta enfermedad afectará a los dos hijos menores, pero no afectará al hijo mayor. La madre y la hija, si se confirma que es portadora, pueden tener algunos síntomas más adelante en la vida. El padre no fue examinado, ya que si tuviera la alteración genética, habría exhibido síntomas de enfermedad en su infancia. En estos casos, las mujeres miembros de la familia, particularmente la madre, son evaluadas para establecer su estado. La posibilidad de que el hijo varón de un portador herede la eliminación (y la enfermedad) es del 50%. Una consecuencia de esta prueba es que la hija comprendería antes de tener hijos su potencial para transmitir la mutación DMD (porque parece ser portadora). ¿Qué bandas corresponden a las regiones del ADN que se eliminan en esta enfermedad hereditaria? Contando desde la izquierda, las bandas tercera, cuarta y séptima no están presentes en el ADN de los hijos menores que padecen esta enfermedad, lo que corresponde a la eliminación de elementos de ADN que codifican regiones de la proteína distrofina. ¿Jean tiene esas bandas, aunque es portadora? ¿Por qué? A Jean le faltan las bandas en el ADN de su hijo menor de su cromosoma intacto, pero su segundo cromosoma lleva la eliminación (recuerde que Jean es XX, y la eliminación está en solo uno de sus cromosomas X). ¿Qué problemas plantea este tipo de pruebas? Este tipo de pruebas plantea una serie de problemas. ¿En qué punto desea un individuo saber su estado? Dado que la hija en este caso parece ser portadora (la misma intensidad de banda que su madre y su hermano no afectado), una pregunta clave es si informarle a la hija sobre su estado, cuándo realizar pruebas adicionales para ella y cómo / cuándo informar a los niños más pequeños que tienen una enfermedad que afectará significativamente sus vidas. ¿Qué impactos surgen en la atención médica debido al diagnóstico definitivo de esta enfermedad? ¿Se verá afectado el acceso a la atención médica? ¿Mejorado? Retenido? El impacto varía en todo el mundo y, por lo tanto, variará en diferentes entornos. Para el individuo, el conocimiento de que la enfermedad se desarrollará y progresará puede ser muy angustiante, y los impactos psicológicos y físicos deben considerarse como parte de las pruebas y el proceso de tratamiento posterior.
0 Comments
Leave a Reply. |
Categories
All
|
 RSS Feed
RSS Feed
